L'ancienne unité est le Curie (Ci). C'est une unité historique découverte par Pierre et Marie Curie
et qui correspond à l'activité d'un gramme de ; en fait, un gramme de à une activité
de 0,989 Ci. Un Ci et égal à 37 GBq soit 37 milliards de désintégrations par seconde.
Trois risques peuvent être définis : l'exposition externe sans contact, l'exposition externe avec contact et l'exposition interne.
Dans ce mode d'exposition, l'individu n'est pas en contact avec la matière radioactive : elle est à l'extérieure de son corps et il ne la touche pas.
C'est le terme qui définie l'irradiation.
Nous retrouverons ce risque d'exposition lors de l'utilisation de sources radioactives sous forme scellée (rayonnement
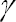
,
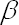
), de générateurs électriques de rayons X (rayonnements X), mais aussi lors de la manipulation de sources non scellées (rayonnements
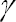
et
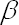
).
Ce risque n'existe pas avec les
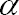
du fait de leur très faible parcours dans l'air.
Une irradiation peut être globale (corps entier) ou partielle (localisée) ; les effets seront d'autant plus graves que la dose sera élevée.
La matière radioactive, cette fois ci, a pénétré à l'intérieur du corps.
C'est le terme qui défini la contamination interne.
Nous retrouvons ce risque d'exposition lors de la manipulation de source non scellées (rayonnement
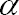
,
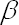
).
Il existe plusieurs voies d'incorporation : l'ingestion, l'inhalation, la pénétration par une plaie ouverte, la pénétration trans-cutanée.
La manipulation des sources non scellées requiert donc une attention toute particulière, même pour les faibles activités. La dosimétrie découlant d'une exposition interne est particulièrement difficile à évaluer car les activités incorporées sont souvent mal connues et dures à mesurer.
Contamination/Irradiation
Il est très important de comprendre la différence entre une contamination (interne ou externe) et une irradiation.
Dans un cas comme dans l'autre, le risque n'est pas dû à la même quantité de matière.
Nous avons vu qu'à l'échelle atomique la matière est constituée de vide, le corps humain également. Les rayons
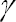
(parcours dans l'eau de quelques m) n'étant pas chargés électriquement ne seront pas attirés par les constituants de la matières (électrons ou noyaux) et devront être très nombreux pour qu'il y ait une probabilité qu'ils entrent en interaction avec eux, donc qu'ils engendrent des modifications chimiques à nos cellules humaines en leur cédant leur énergie.
Par contre, les
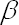
(parcours de quelques mm dans l'eau) et à plus forte raison les
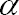
(parcours de quelques mm dans l'eau), lorsqu'ils sont ingérés, vont générer des modifications chimiques au sein de nos cellules dés les plus faibles quantités.
C'est pourquoi, une faible quantité de matière peut être dangereuse en ingestion et ne représenter qu'un risque très faible du point de vu de l'irradiation.
Ce risque est bien représenté par les champignons contaminés suite à l'accident de Tchernobyl. Ne présentant pas de risque lorsqu'ils sont à l'extérieur ne notre corps, ils deviennent dangereux en cas d'absorption.
De même, les vapeurs d'une cuillère à soupe d'eau de Javel concentrée paraissent bien inoffensives au vu des dégâts occasionnés en cas d'ingestion.
Haut de Page

Les moyens de protection.
Les moyens de protection sont simples ; leur but est d'éviter une exposition qui engendrera une dose.
Il en existe quatre :
- l'activité
- le temps
- la distance
- les écrans
L'exposition externe avec contact
C'est un moyen de protection particulier et qui n'est pas utilisable de manière facile.
Tout d'abord, lorsque l'on acquerra une source radioactive, le constructeur de l'équipement dimensionnera la source, en activité, de manière optimale. De telle sorte, l'on a peu d'influence par rapport à l'activité.
Par contre, l'abaissement de l'activité est une technique utilisée dans les centrales nucléaires. Lors d'un arrêt pour changement de combustible, avant intervention des opérateurs, l'exploitant se charge de rincer les circuits, notamment le circuit primaire, afin d'abaisser l'activité et donc les débit d'équivalent de dose ; cela permet de diminuer la dosimétrie individuelle, mais également collective. Cependant cette activité n'est pas éliminée, elle est seulement concentrée dans des filtres qui deviennent donc extrèmement radioactifs.
Dans les laboratoires où sont utilisées des sources non scellées, celles ci étant toujours composées de radioéléments à vie courte (période de l'ordre du jour ou du mois), les déchets sont gérés grace à la baisse d'activité du à leur décroissance radioactive. L'on considère alors, car les activités manipulées sont faibles, (quelque kBq à quelque MBq) qu'il faut attendre 10 périodes pour retrouver un radioactivité proche de la naturelle (soit une réduction de 210 ou de 1024 fois l'activité initiale). Les déchets sont alors considérés comme des déchets chimiques classiques et sont éliminés comme tels.
Il est à noter que dans le cas énuméré ci-dessus, c'est surtout le facteur temps qui est pris en compte.
Le temps
C'est un facteur qui va déterminer de façon importante la dose. Il est très facile de comprendre que plus le temps sera long, plus la dose intégrée sera importante. Exposé à un débit de dose de 50 mSv/h durant ½ h, un individu intégrera une dose de 25 mSv. S'il reste 2 h, sa dose sera alors de 100 mSv.
La dose est donc strictement proportionnelle au temps : débit x temps = dose.
Il est absolument inutile et malvenu de stationner sans raison dans une ambiance radioactive, si faible soit elle ; de plus il est essentiel d'optimiser son temps de séjour à proximité de matériel radioactif.
La distance
Elle joue un rôle identique au temps et logiquement, plus l'on s'éloigne de la source, plus le débit de dose diminue.
Cependant deux cas de figure peuvent se présenter :
- la source est ponctuelle (assimilable à un point)
- la source est linéaire (assimilable à une ligne)
Source ponctuelle
L'on dit qu'une source est ponctuelle lorsque la distance à laquelle on se trouve par rapport à elle est au moins égale à 5 fois son diamètre. En industrie, la plupart des sources scellées utilisées sont ponctuelles.
Dans le cas de sources ponctuelles, le débit de dose est inversement proprtionnel au carré de la distance.
En effet, une source radioactive émet en 4Pi, c'est à dire dans toutes les directions de l'espace ; elle libérera donc son énergie de manière spatiale. Ce phénomène n'est pas propre à la radioactivité mais se rencontre également dans d'autres domaines comme le bruit, la lumière
Le shéma ci-dessous illustre bien l'influence de la distance pour une source ponctuelle.
Schema diminution débit
Il apparaît donc que si l'on double la distance, l'énergie d'une source donnée n'est plus dissipée sur une surface de 2 fois quatre carreaux, mais sur une surface de 4 fois quatre carreaux. Le débit de dose sera diminué d'un facteur 4 et non d'un facteur 2. Si l'on triple la distance, l'on diminuera d'un facteur 32, soit 9.
Il est donc assez facile de se protéger d'une source ponctuelle en utilisant la distance qui décroîtra rapidement, mais à l'inverse, le débit de dose va croître de façon exponentielle lorsque l'on se rapprochera : il est donc strictement interdit de toucher une source radioactive avec les doigts, même si celle ci est de faible activité.
Source linéaire
Une source linéaire est tout simplement une succession de sources ponctuelles. En fait, dans l'industrie, on rencontre peu de sources linéaires. Dans une centrale nucléaire, une source linéaire peut prendre forme dans une tuyauterie lorsque celle-ci se remplit de boue radioactive par exemple. L'industrie chimique utilise des sources linéaires pour mesurer des niveaux. Dans ce cas là, la diminution du débit de dose est strictement proportionnelle à l'augmentation de la distance : on double la distance, on diminue le débit de dose d'un facteur 2. Il est beaucoup plus difficile (par rapport à une source pontuelle) de se protéger d'une source linéaire en jouant sur la distance.
Haut de Page

©Dom - 2002 ekinimod@online.fr - MàJ le: 03 Mar. 2003


![]()
![]()


![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()